﮵������˥���仯��ԭ�����
ʱ��:2021-05-20 10:34��Դ:﮵�ǰ�� ����:�ۺϱ���
���:
��
һ��������������˥���������
�����������Һ����Ĥ���������ӵ�ص���Ҫ�ɷ֡�����ӵ�ص��������ֱ���﮵�Ƕ���ѳ���Ӧ������������Ƕ�����ΪӰ������ӵ����������Ҫ���ء���ˣ�����ά������ӵ��������������ƽ���ԣ�����ȷ����ؾ߱�������ܡ�
ͨ����˵������ӵ�س����л��ܼ��͵���ʣ���Σ���ɵĵ������Һ���õ������ҺӦ���߱��㹻�ĵ����ԡ��ȶ��ԣ������ܹ���缫ʵ�����ݡ����ڸ�Ĥ��˵���������Ǿ���������輰����ṹ����Ҫ���أ��Ե������˥���仯�������ֱ�ӵ�Ӱ�졣����Ĥ��������������Խ������������������ӵ�ص��������ۺ����ܡ�һ������£���Ĥ�ڵ������Ҫ���ŷָ���������͵�ظ��������ã����������������Ӵ������µ�ض�·��ͬʱ���ܹ����е�������ӣ��Գ�ַ��ӵ��Ч�á�
����ӵ���еĻ�ѧ��Ӧ���������������Ƕ����ѳ������е�������ԭ��Ӧ�����������縺������SEIĤ���������ƻ������Һ�ķֽ��Լ����Բ��ϵĽṹ�仯���ܽ�ȸ���Ӧ����Щ����Ӧ�����������ӵ������˥����ԭ��
���ѭ�������з�������˥������ʧ�DZ�Ȼ������ˣ�Ϊ����ߵ�����������ܣ�������������ѧ�߳���о���﮵��������ʧ�Ļ�����Ŀǰ����֪��������ӵ������˥������Ҫ���ذ��������������γ�SEI�ۻ�Ĥ������﮳������缫���Բ��ϵ��ܽ⡢������������ԭ��Ӧ��Ӧ�ķ������ṹ�仯����仯�ȡ���ǰ��������ӵ������˥���仯����ԭ����Ȼ�ڲ����о��Ĺ����С�
���������
2.1 �������䷴Ӧ
�ܹ���Ϊ����ӵ�ظ����Ļ��Բ�������϶࣬��̼ϵ�������ϣ�����������������ϡ�����﮸������ϵ�Ϊ��Ҫ���ϡ���ͬ���͵�̼���Ͼ��в�ͬ�ĵ绯ѧ���ܣ����У�ʯī���е������ܽϸߡ���״�ṹ�������ᾧ�ȸߵ����ƣ���Ϊ�ʺ�﮵�Ƕ����ѳ���ͬʱʯī���ϼ۸�ʵ�ݡ������϶࣬��ˣ�Ӧ�ý�Ϊ�㷺��
������ӵ���״γ�ŵ�ʱ���ܼ����ӻ���ʯī���淢���ֽⷴӦ�����γ���ΪSEI�Ķۻ�Ĥ����һ��Ӧ���������������ʧ���������ڲ�����Ĺ��̡�����ӵ�ع��������У���������ᷢ������﮳�������������������������Բ�������ڸ������Բ��Ϲ���������¡�ͬʱ�����ڸ߱��������£�Ҳ�п��ܲ�������﮳�������
ͨ����˵���γɽ���﮵���﮵������˥���仯��ԭ����Ҫ�������·��棺��һ�����µ���п�ѭ��������ͣ��ڶ�������������ʻ��ܼ���������Ӧ���γ�����������������������Ҫ�����ڸ�����Ĥ֮�䣬�Ӷ���ɸ�Ĥ��϶���������µ���������ӡ�ʯī���ϵIJ�ͬ������ӵ������˥���仯��Ӱ�����Ҳ����һ�����졣��Ȼʯī�ıȱ�����ϸߣ���ˣ������Էŵ練Ӧ���ᵼ��﮵��������ʧ��������Ȼʯī��Ϊ��ظ�������绯ѧ��Ӧ�迹Ҳ������ʯīҪ�ߡ����⣬ѭ�������и�����״�ṹ���롢��Ƭ���������е������ɢ�������������е绯ѧ��Ӧ�迹�����ӵ����أ����ǵ���﮵��������ʧ����Ҫ���ء�
2.2 �������䷴Ӧ
�����������Ҫ����������ռ�ȹ��͵�����·��������µ缫������ʧ�⣬��ʹ﮵�������������������ʧ�������������Ϻ͵��Һ�ֽ��������������ȼ����IJ���Ͳ��ϻ��ۣ����ܻ��﮵�ص�ʹ�ô�����ȫ������
2.3 ���Һ�ڸߵ�ѹ�·�����Ӧ
��﮵�س���ѹ���ߣ����ᵼ�µ��Һ����������Ӧ�������ɲ��ָ�������缫�������谭������ӵ�Ǩ�ƣ��Ӷ����ѭ������˥���仯�������Ũ�Ⱥ͵��Һ���ȶ��Եı仯���Ƴɷ��ȣ������Ũ��Խ�ߣ����Һ�ȶ���Խ�ͣ�����������ӵ����������Ӱ�졣�ڳ������У����Һ�ᷢ��һ�����ģ���ˣ���Ҫ��װ��ʱ���в��䣬���µ�ػ��Բ��ϼ��٣���Ӱ���س�ʼ������
�������Һ�ֽ�
���Һ��������ʡ��ܼ������Ӽ��������ʻ�Ե�ص�ʹ�����ޡ������������ʳ�ŵ����ܺͰ�ȫ���ܵȲ���Ӱ�졣���Һ�е���ʺ��ܼ��ķֽⶼ������������������ʧ�����״γ�ŵ�ʱ���ܼ��������ڸ�����������SEIĤ���γɲ������������ʧ�������DZ�Ȼ����������Һ�д���ˮ������������ʱ�����ܻ�ʹ�����LiPF6���¶Ƚϸߵ�����·����ֽ⣬�������ɵIJ������������Ϸ�Ӧ�����µ�������ܵ�Ӱ�졣ͬʱ�����ֲ��ﻹ�����ܼ�������Ӧ�����Ը�������� SEIĤ���ȶ������Ӱ�죬���������ӵ������˥��������֮�⣬�����Һ�ֽ�IJ��ﲻ����Һ���ݣ�������Ǩ�ƹ���������������϶���Ӷ����µ������˥�����ܵ���˵�����Һ�͵�ص�������֮�丱��Ӧ�ķ������Լ������ĸ����������ɵ������˥������Ҫ���ء�
�ġ��Էŵ�
����ӵ����һ������£��ᷢ���������������һ���̱���Ϊ�Էŵ磬��Ϊ����������ʧ�Ͳ�����������ʧ���ܼ��������ʶ��Էŵ����ʲ���ֱ��Ӱ�죬���������Բ��Ͽ����ڳ������к����ʷ�����Ӧ�����������Ǩ���������ʧ�⼰������˥������ˣ����Կ������ٻ��Բ��ϱ�������Խ���������ʧ���ʣ����ܼ��ķֽ��Ӱ�����������������⣬��Ĥ©��Ҳ�ᵼ��������ʧ�������ֿ����Խϵ͡��Էŵ����������ڴ��ڣ��ᵼ�½���﮳���������һ������������������˥���仯��
�塢�缫���ȶ���
�������У���������Ļ��Բ��ϲ��ȶ����ᵼ���������ʷ�����Ӧ����Ӱ�������������У��������Ͻṹȱ�ݡ������ƹ��ߡ�̿�ں�������Ӱ������������Ҫ���ء�
5.1 �ṹ���
5.1.1 LiMn2O4
�⾧ʯLiMn2O4���ҹ����зḻ��Դ���Ҽ۸���������нϺõ����ȶ��ԣ��ǵ����������Ҫ���ϡ�LiMn2O4�����ڸ��»����µĴ��漰��س�ŵ�ѭ�������У����ᵼ�µ����������˥���仯������Ҫ�����������ص��µģ����ȣ��ڸߵ�ѹ�����£����Һ�����绯ѧ��Ӧ��һ���Ǹ���4.0V����Σ�LiMn2O4�����к��е�Mn�ڵ��Һ���ܽ⣬�����绯��Ӧ���ƻ����������ϵľ���ṹ��
������LiMn2O4Ϊ������CΪ����������ӵ�أ�����ڸ�ѹ״̬�µ����ܼ������ֽ⣬��������C������������Ӧ�����ɵ�������������������Ǩ�ƣ����������������ܽⷴӦ���ܽ���γɵĶ��������ӽ����ڸ�������ԭ�������������ʹ�ͬ��������Mn��������ֻ���ڸ���������Ĥ�ķ���������������������ڿ���������ķ���Mn���������������SEIĤ�ı��棬Ҳ����Ϊ�������Żᵼ�µ����������˥���仯�������Ƽ�������Һ�У��ܹ���Ч�Խ������ӵ��ܽ�״̬�γ��������ã���������ص�ѭ�����ܡ�
����֮�⣬��LiMn2O4Ϊ������CΪ����������ӵ���ڳ�ŵ�����У���������ӵ�Ƕ����ѳ������ܻ�����LiMn2O4�ľ������仯������������ϵ���ķ���ϵ�䷢����ת�䡣����������������ڲ�����ɢ���ʱ�����������������Ƕ������Ҫ�ͣ�����λԼΪ4Vʱ������Ӿۼ���LiMn2O4���棬������Jahn-TellerЧӦ����ʹ�ṹ����Ť����ת�䣬�Ӷ�����������˥����
5.1.2 LiCoO2
LiCoO2������ӵ�����������е�Ӧ�þ��нϴ����ƣ���Ҫ�������ܹ������ʵ������ӵ�Ƕ������룬���Ҿ��нϴ���������ɢϵ����������������ṹ�仯�̶ȣ���ˣ���������﮵�س�ŵ����������Ҫ���á�ͬʱ���ò��Ͻṹ�ȶ�������ӵ���Ƕ�����ԽϺã��ܹ���Ч��֤��ŵ�Ŀ���Ч�ʼ���ص�ʹ�����ޡ�ͨ�����������ѧ�߶�LiCoO2��ϵ������˥���������о�������Ӱ��﮵��ѭ������������˥���仯��������Ҫ���������������迹���ߺ�����������ʧ��
ͬʱ�����ѧ�����֣�ѭ������Խ�ߣ�������������������ʧ��ȫ���������ʧ��ȹ����ͣ��һ��������Ǩ���������½�����Ե����������˥�����������Ӱ�졣������ͼ1��֪�����ѭ��������200�κ��������ϲ�δ������䣬 ��LiCoO2��״�ṹ�����̶Ƚ��ͣ�����ӡ������ӵĻ����������ӣ�ʹ�������������Ч��Ƕ���Ӷ����µ������˥�������⣬���ӷŵ籶�ʻ��ﮡ���ԭ�ӵĻ�ϲ����ٽ����ã��ᵼ�� LiCoO2 ԭ�е���������ת��Ϊ�������ͣ��Ӷ���������ӵ�ص�����˥���仯��
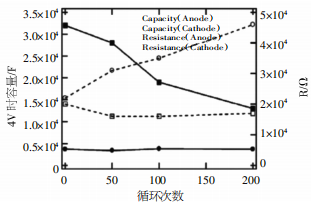
ͼ1 ѭ���������迹�������仯����
���⣬��LiCoO2��ϵ�У�ͨ����25�棨������״̬�£���60���е��ѭ������˥�����ɵ��о����ɷ�����150��ѭ��ǰ��60�����µ�طŵ�����Ҫ�ȳ����µ�������Ͷ�����ߣ�������Ϊ�ڸ���״̬�µ��Һ�Ƚ��ͣ�ʹ�����Ǩ�������������Ӷ������﮵������ʣ���ر��ֳ��ϸߵij�ŵ�������������300��ѭ����60���µ�صļ���������ʧҪԶ���ڳ���״̬�£����Կ����¶����Ӿ�������ӵ�س�ŵ�����е缫�ĵ绯ѧ������ʹ��﮵���ڳ�ŵ������������ʧ��Ϊ���ء�
5.1.3 LiFePO4
LiFePO4����Դ�㷺���۸���ˣ����������õ��ȶ��Ͱ�ȫ���ܣ��ܹ��ﵽ170mAh/g�����۱�������������ȹ��ʺͱ�������LiCoO2������ܹ�ʵ����������Һ���������ݣ���ˣ����㷺Ӧ����﮵�����������ô��ֲ��ϣ��Ե��������Ӱ��������Ҫ�����������㣺һ������������֮�䷢������Ӧ����ʹ��ѭ��﮵ļ��٣������ƻ���������֮���ƽ�⣻�������ڽṹ�ӻ����缫���롢�����ܽ⡢�������������أ����»��Բ��ϲ�����ʧ���Ӷ�Ӱ����������
5.2 �������ϵ�̿�ں���
����̿�ڱ����Ƿǻ������ʣ���˲�����ŵ練Ӧ������������������̿�������ߣ�������������ϵ�ǿ�ȼ���������Ӱ�죬������Ҫ�������ӡ����⣬����������̿�ڱ��������˾��д����ʵ����ʣ����ܹ������������ӷֽ����ʣ����ܹ���Ч�ٽ����������ܽ⡣
�����ܽ�
��������������ӵ�����ھ����������ܡ���Ⱦ�ϵ͵�“��ɫ���”�����㷺Ӧ�����ҹ����и�ҵ֮�У�������ӵ�ص�ʹ���������ܵ��������Ͻṹ��̿�ں������缫�ȶ��ԡ��Էŵ硢����������ӡ�����ʷֽ�����ص�Ӱ�죬���µ������˥�����졣
�ο��������ȡ�����ӵ������˥���仯��ԭ�������
�������������Ľ��������߸��˹۵㣬���й���������ء���ԭ�����Լ����г������ֺ�����δ������֤ʵ���Ա����Լ�����ȫ�����߲������ݡ����ֵ���ʵ�ԡ������ԡ���ʱ�Ա�վ�����κα�֤���ŵ������߽����ο����������к�ʵ������ݡ�
������ע�� ����Դ��XXX�����й�������ˣ�������Ʒ����ת��������ý�壬ת��Ŀ�����ڴ��ݸ�����Ϣ����������������ͬ��۵�Ͷ�����ʵ�Ը���
������Ʒ���ݡ���Ȩ������������Ҫͬ������ϵ�ģ�����һ���ڽ��У��Ա����Ǽ�ʱ������
QQ��503204601
���䣺cbcu@cbcu.com.cn
������ע�� ����Դ��XXX�����й�������ˣ�������Ʒ����ת��������ý�壬ת��Ŀ�����ڴ��ݸ�����Ϣ����������������ͬ��۵�Ͷ�����ʵ�Ը���
������Ʒ���ݡ���Ȩ������������Ҫͬ������ϵ�ģ�����һ���ڽ��У��Ա����Ǽ�ʱ������
QQ��503204601
���䣺cbcu@cbcu.com.cn
����ϲ��
-
����ION��˾��̬�����ͻ�ƣ���125��ѭ��������˥������5%
2024-03-11 22:56 -
����ӵ�ظ�Ĥ����Ҫ���ܲ�������Щ��
2023-01-24 18:18 -
���������﮵�ò�Ʒ�Ƿ�һ���ܰ﹫˾ҵ�����֣�
2023-01-24 18:16 -
﮵��ҵ��������Ӿ����ϵͳ������Ч��
2023-01-24 18:11 -
��ԣ�Ƽ���3��ԪͶ��﮵������������Ŀ
2023-01-10 15:53 -
Ǧ�ᡢ���ӡ����⡢﮵����ȱ��Ա�
2022-06-21 08:42 -
Ԥ﮻�������﮵�����ж���Ҫ
2022-04-06 10:40 -
ȼ�ϵ�ص�˥������
2022-04-01 10:25 -
���ǵ�����õ�Ƭ��س���ٶȱ���Ԫ﮵�ػ��죿
2021-08-19 09:09 -
PPT | ﮵�ع�̬����ʵ��о�
2021-06-16 11:41
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ר��
�������
-
����ION��˾��̬�����ͻ�ƣ���125��ѭ��������˥������5%
2024-03-11 22:56 -
����ӵ�ظ�Ĥ����Ҫ���ܲ�������Щ��
2023-01-24 18:18 -
���������﮵�ò�Ʒ�Ƿ�һ���ܰ﹫˾ҵ�����֣�
2023-01-24 18:16 -
﮵��ҵ��������Ӿ����ϵͳ������Ч��
2023-01-24 18:11 -
��ԣ�Ƽ���3��ԪͶ��﮵������������Ŀ
2023-01-10 15:53 -
Ǧ�ᡢ���ӡ����⡢﮵����ȱ��Ա�
2022-06-21 08:42 -
Ԥ﮻�������﮵�����ж���Ҫ
2022-04-06 10:40 -
ȼ�ϵ�ص�˥������
2022-04-01 10:25
�����ȵ�
-
2024﮵�����б���
2024-05-24 18:59 -
С����ֵ�����죬������ʱ���������ʹ�˾��
2024-05-20 19:05 -
���﮵���Ŀ��ֹ���ذ��ļ�������ҵ����������ܣ�
2024-05-15 19:12 -
Я�ֶ�������������ҵ5����������Ŀ����/ǩԼ!
2024-05-21 18:46 -
�ذ�������Դͻ���������ã���̬���������������
2024-05-28 18:18 -
Ͷ�ʳ�25��Ԫ�����﮵���ҵ�������������ػ�ѧƷ��Ŀ
2024-05-22 19:20 -
��һ10GWh��Ŀ��������̬��ؾ����ҵ����Ҫ��ã�
2024-05-11 19:17 -
����ʱ�������ǵϡ��д��º���ͬ����ε�����ֵ�����
2024-05-09 18:48


©2017 ��Ȩ���� ��ɫ�ǻ���Դ�����о�Ժ ������̩�Ƽ�������������˾ �а� Power by DedeCms
��ֵ�ɾ���ҵƷ�ƣ��߳�Ϊ���ṩ�������ȵ���Ѷ
��ICP��2024061100��
��ֵ�ɾ���ҵƷ�ƣ��߳�Ϊ���ṩ�������ȵ���Ѷ
��ICP��2024061100��
 �Ź��ں�
�Ź��ں�







