-60℃正常工作的电池不香吗?复旦大学彭慧胜:超低温Li-CO2电池
时间:2020-05-22 10:11来源:高分子科学前沿 作者:综合报道
点击:
次

研究背景
非质子化Li-CO2电池由于具有较高能量密度(1876 WhKg-1),且耦合了有效CO2固定和先进储能的双重特征,引起了储能领域的高度关注。此外,由于阴极材料是空气中的CO2,Li-CO2电池在航空航天探索技术中表现出独特的优势。例如,火星大气层中CO2的浓度高达96%,是未来Li-CO2电池最有前途的应用领域。为推进Li-CO2电池的实际应用,近年来研究人员开发了各种催化阴极、电解质添加剂和准固态固态电解质,并设计新的柔性电极,来提高Li-CO2电池能量/功率密度、循环性能和机械柔性。虽然该领域已经取得了阶段性的进展,但是现有的研究工作中Li-CO2电池的工作环境主要集中在室温到150℃高温下。而火星是一个极冷的行星,平均温度约为零下六十度,目前所报道的Li-CO2电池在极端寒冷的环境下无法正常工作。众所皆知,环境温度的降低会导致电解质电导率降低,电极反应动力学变慢,电极/电解质界面变差,因此需要使用更多的能量来驱动放电和充电过程,从而增加了放电/充电过程中的过电势,缩短了循环寿命。更糟糕的是,由于电解质完全凝固,电池将无法在超低温(如-60℃)下正常工作。到目前为止,还没有关于低温(零度以下)Li-CO2电池的研究,更别说超低温Li-CO2电池了。
成果简介
为应对上述挑战,复旦大学高分子科学系彭慧胜教授和王兵杰教授设计并组装了一种Swagelok型Li-CO2电池。该电池使用金属锂为阳极材料,含LiTFSI的1.3-二氧戊环(DOL)为电解质,涂有铱催化剂的气体扩散层作为阴极,并采用市售的Parafilm作为阴极保护层。得益于DOL基电解质在低温下的超低凝固点,高离子电导率和良好的电化学稳定性,以及铱阴极对CO2还原反应(CO2RR)和CO2析出反应(CO2ER)的高催化活性,所制备的Li-CO2电池可以在超低温环境下高效工作。在电流密度为100 mAg-1和-60℃的超低温下,电池表现出8976 mAg-1的高深度放电容量和150个循环(1500 h)的超高循环寿命,且每个循环的固定容量为500 mAg-1。低温下如此优异的电化学性能得益于阴极上形成小尺寸易分解的放电产物以及电解质和锂阳极上抑制副反应的产生(图1)。相关成果以“Li-CO2Batteries Efficiently Working at Ultra-Low Temperatures”为题于2020年5月15日发表在Advanced Functional Materials上。
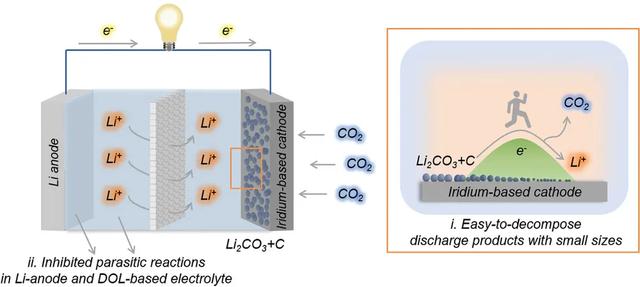
图1. Li-CO2电池在超低温环境下工作的原理示意图以及在放电(左侧)和充电(右侧)过程中放电产物的形成和分解。Li-CO2电池的工作机理基于电化学反应4Li + 3CO2 + 4e− ⇋2Li2CO3 + C(E = 2.80 V vs Li + / Li)。
图文详解
一、超低温Li-CO2电池的设计
超低温电池的设计通常涉及系统的材料选择和/或电池结构的优化。首先应使用高导电性的电解质,以确保其在低温下有效的离子传输和良好的电解质/电极界面。DOL是一种小的环状醚分子,具有-95℃的低冰点,低粘度和溶剂化锂离子的去溶剂能低等良好特性,并且容量大,可确保锂阳极的高循环效率。因而,成为超低温Li-CO2电池电解液的理想候选者。与普通的四甘醇二甲醚基电解质(约-40℃)相比, DOL基电解质的凝固点甚至低于-100 ℃,且具有更高的离子电导率,在-80℃时能够保持2.26 mS cm−1的高电导率。此外,由于增强了电解质的稳定性,DOL的引入可以有效抑制电解质中副反应的产生。电解质的氧化稳定性随温度的降低而提高,其稳定的电压范围从0℃时的3.05 V增加到−30°C时的3.53 V和−60°C时的4.34 V。因此, DOL是一种理想的低温Li-CO2电池的电解质溶剂。
由于铱对CO2RR和CO2ER具有较高的催化活性,并已被用于改善Li-CO2电池的电化学性能。因此研究人员选择涂有铱的GDL被用作Li-CO2电池的阴极,并首次探究其在低温储能装置中的性能。另外,考虑到Li-CO2电池是半开放式系统,其电解质不可避免地会通过其多孔阴极连续蒸发。因而,研究人员采用市售的可透过Li-CO2气体的Parafilm材料用作阴极保护层,以抑制电解质的挥发,并进一步延长了Li-CO2电池的使用寿命。
二、Li-CO2电池的低温电化学性能
研究人员首先探究了温度对Li-CO2电池电化学性能的影响。在截止电压为2.0 V,电流密度为100 mAg-1的条件下,Li-CO2电池的深放电容量在0℃时高达14 720 mAhg-1,甚至在-60℃时仍可达到8976 mAhg-1(图2a)。此外,即使在-60℃时电流密度从50 mAg-1增加到500 mAg-1,Li-CO2电池也没有出现明显的电压降,进一步显示出其较高的低温适应性和良好的倍率性能。循环伏安法测试表明,电解质的氧化稳定性随着温度的降低而提高,这使得DOL基电解质能够承受-60℃超低温时的电荷极化。
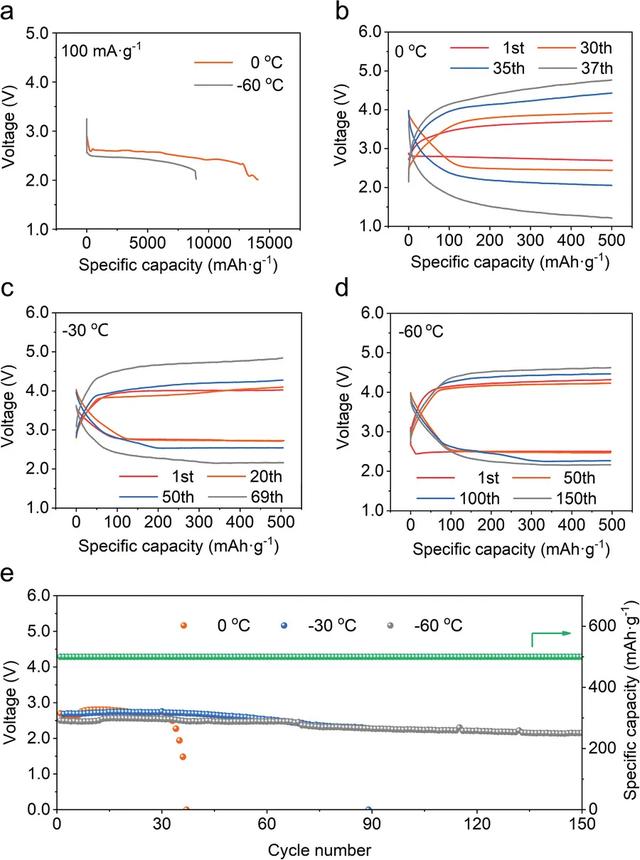
图2. Li-CO2电池在超低温环境下工作的电化学性能。
随后,研究人员对Li-CO2电池在0, -30和-60℃低温下的长期循环稳定性(图2b-d),测试条件:截止容量500 mAhg-1,电流密度为100 mAg-1。在0℃时,Li-CO2电池首次循环表现出0.85 V的中等容量电势差,在第30个循环增加至1.35 V,并在40个循环后最终失效。出乎意料的是,尽管在第一个循环中不可避免地会出现极化间隙扩大现象,但Li-CO2电池随环境温度的降低却表现出增强的循环稳定性。当工作温度降至-30℃时,电池可以稳定地进行69个充放循环,在-60℃时其使用寿命甚至可以延长至150个循环(1500 h)。此外,研究发现铱催化剂的引入,使得极化间隙显着减小,循环次数显着增加。在-60℃的条件下,带有铱涂层阴极的Li-CO2电池可以达到150个循环,而没有铱涂层的Li-CO2电池循环23圈后失效。以上结果表明,基于铱阴极的Li-CO2电池在超低温下可作为一次或二次电池稳定工作,这也是迄今为止首个能在如此超低温下具有高电容和良好循环性的非质子Li-CO2电池。
三、低温下的Li-CO2电池放电产物分析
通常,质子惰性金属气体电池的循环寿命与放电产物的形态和组成密切相关。为探究为什么Li-CO2电池在低温下具有增强的循环性能,研究人员对电池循环后的放电产物进行了分析。非原位XRD和FTIR表征显示,电池的放电产物为碳酸锂(Li2CO3)且充电后在阴极完全分解。这表明所制备的Li-CO2电池在-60℃的超低温下具有良好的可逆性。此外,通过在超低温环境下充电过程中的原位差分电化学质谱分析证实,在充电阶段主要发生了Li2CO3 和C的共氧化反应和Li2CO3的轻微自分解反应:2Li2CO3 + C→4Li ++ 3CO2 + 4e-和2Li2CO3→4Li ++ 2CO2 + O2- + 3e-。
SEM表征显示,放电产物的形态也会随温度而显着变化。在0℃进行初始放电后,循环后的阴极被尺寸为100-300 nm的薄片覆盖(图3c)。随着温度进一步降低到-30和-60℃,产物逐渐演变成直径为50-70 nm(图3d)和30-50 nm(图3e)的球形颗粒。片状和颗粒状产物的产生表明放电产物的形成可能遵循溶液增长机制,而不是表面介导的途径。SEM图像进一步显示,在不同温度下首次充电后,颗粒状的放电产物均已从阴极完全分解去除(图3f-h)。然而,经过十次充放循环后,在0℃下仍有一些未分解的产物在阴极表面残留,而在-30和-60℃下,放电产物完全分解。这说明放电产物的形态和结构极大地影响了Li-CO2电池的可逆性和寿命。
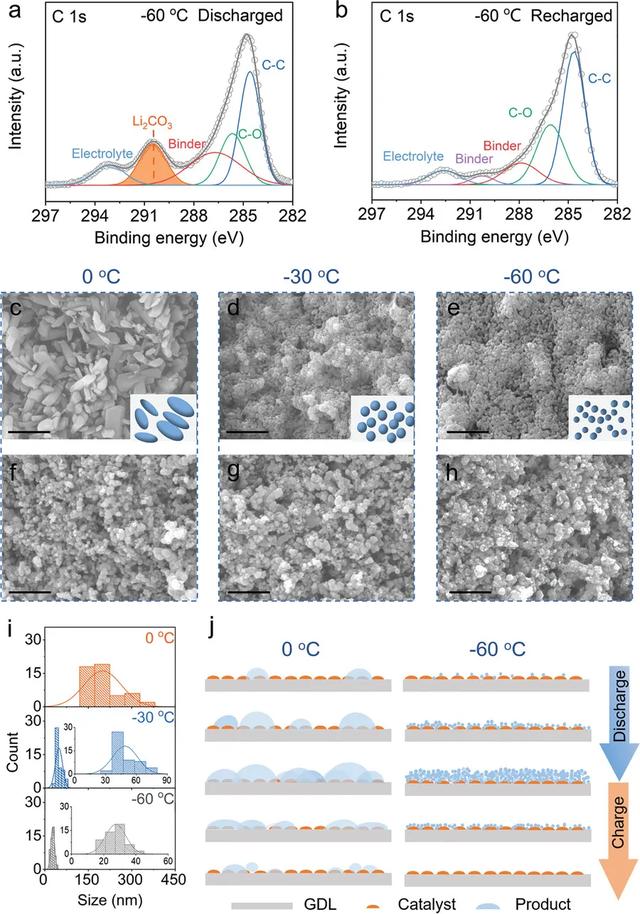
图3. Li-CO2电池在超低温环境下放电产物的形貌以及循环可逆性表征。
因此,研究人员根据放电产物在不同温度下的形貌差异,阐述了低温下Li-CO2电池的循环性能得到改善的原因(图3j)。在−60°C的低温下,产物的成核比在0°C的情况下更容易发生。而在−60°C的条件下,放电产物的生长过程变慢,从而导致更小的颗粒状产物在阴极上松散地聚集,而在0°C放电结束时较大的产物颗粒沉积在电极表面上。此外,由于电子隧穿距离的限制,绝缘产物的氧化通常从溶液固相间区域向绝缘体内部进行。由于界面和氧化位的增加,使得小尺寸的产品颗粒更易于在充电过程中分解。而Li-CO2电池的“死亡”与循环时阴极上未分解的绝缘产物的积聚有关,这将导致多孔阴极的堵塞和钝化。因此,低温下形成的放电产物尺寸更小更容易分解,并且在充电后能够完全分解,这极大地提高了电池的可逆性和循环性能。
四、Li-CO2电池低温下的稳定性
除了未分解的放电产物积聚在阴极上,循环过程中产生的不良副反应也是金属气体电池过早失效的重要原因。为了验证这一点,研究人员通过使用新的锂片来重新激活失效的Li-CO2电池,并对新鲜和循环后的电解质以及对循环前后的锂阳极分别进行了非原位1H核磁共振分析和 XRD表征。核磁共振谱显示(图4a–c),没有明显证据表明重新收集的电解液在−30和−60°C时发生了不良反应,而在0℃下十个循环后电解液出现了严重的副反应,包括DOL分子的分解和开环聚合。这些结果表明,较低的环境温度能够有效地抑制一些与DOL电解质有关的不良反应。
同样,X射线衍射图表明,在0°C下经过十个循环后,锂阳极表面出现了不良的水合锂(LiOH)副产物,这可能是由于锂阳极与水分或电解质的反应所致。相比之下,在−30和-60°C循环的Li阳极上没有可检测到的LiOH信号(图4d-e),证明在较低温度下,Li阳极上的一些不良副反应被抑制了。另外,除了提高电解质的稳定性外,低温下电池中水含量的降低也可能有助于改善Li-CO2电池的循环性。实际上,即使在最初的电池组装过程中使用了完全干燥的材料,由于环境水的进入和电解质的降解,在长期操作过程中仍然很难从电池中完全去除水分,这不可避免地会引起不必要的副反应,从而缩短了电池寿命。但是,由于水分减少甚至不存在,以及电解质的稳定性增强,这些与水分有关的副反应在超低温下可能会受到抑制。总的来说,降低工作温度可有效抑制Li-CO2电池中有害的副反应,这也是改善低温循环性能的另一个重要因素。

图4. Li-CO2电池电解液和锂阳极在不同温度下循环的稳定性分析。
五、低温下Li-CO2电池的应用演示
考虑到Li-CO2电池最有可能在火星上找到重要的应用,研究人员对超低温Li-CO2电池进行了概念验证。如图5a所示,Li-CO2电池在超低温环境中利用CO2并输出稳定的电压,即在−70°C的超低温环境( 通过干冰实现)中为宇航员模型上的发光二极管供电。图5b-c均证实了Li-CO2电池可用于在低温环境中为电子设备供电。此外,根据火星在一段时间内的实际温度波动而改变环境温度,电池仍然可以在稳定工作,电压几乎没有变化(图5d)。
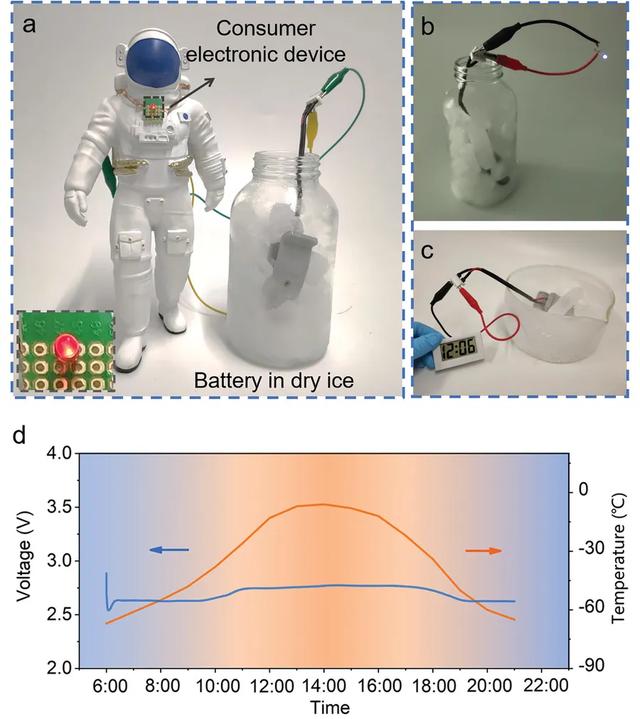
图5. 超低温Li-CO2电池的应用演示。
小结
总而言之,该工作首次实现了高效的超低温Li-CO2电池,不仅可以在-60℃超低温环境下稳定运行,而且具有高达8976 mAg-1的高深度容量,使用寿命长达150次循环(1500小时)且每圈固定容量为500 mAhg-1。研究表明,在超低温环境下增强循环稳定性主要归功于阴极上小尺寸易分解放电产物的形成以及低温对电解质和阳极上副反应产生的抑制。这项工作为开发在超低温下运行的高性能金属气体电池提供了一个通用而有效的范例。
参考文献:Li-CO2 Batteries Efficiently Working at Ultra-Low Temperatures. Adv. Funct. Mater. 2020, 2001619. DOI:10.1002/adfm.202001619
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/adfm.202001619
免责声明:本文仅代表作者个人观点,与中国电池联盟无关。其原创性以及文中陈述文字和内容未经本网证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。
凡本网注明 “来源:XXX(非中国电池联盟)”的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。
如因作品内容、版权和其它问题需要同本网联系的,请在一周内进行,以便我们及时处理。
QQ:503204601
邮箱:cbcu@cbcu.com.cn
凡本网注明 “来源:XXX(非中国电池联盟)”的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。
如因作品内容、版权和其它问题需要同本网联系的,请在一周内进行,以便我们及时处理。
QQ:503204601
邮箱:cbcu@cbcu.com.cn
猜你喜欢
-
韩国研发单原子铂催化剂 可让燃料电池在700摄氏度高温下工作
2020-11-06 09:48 -
研究团队探讨固态电池工作极限 以提升电动汽车续驶里程
2020-11-03 09:03 -
-60℃充电!高性能低温锂金属电池
2020-09-21 11:59 -
美国研发可在零下10摄氏度工作的锂金属电池
2020-08-25 17:33 -
斯坦福研发阻燃固态电池:着火后依然正常供电
2020-03-15 15:22 -
青岛能源所揭示出下一代锂金属电极的工作机制
2019-12-18 10:48 -
科学家提出新型预锂化策略用于提升锂离子电池在宽工作温区下的性能
2019-10-21 21:33 -
研究人员研发新型电解质 扩大锂离子电池的工作温度范围
2019-07-11 10:29 -
新材料“极温电池”-55℃正常放电 寿命超8年
2018-09-10 14:46 -
深圳先进院等研发出可在室温下稳定工作的新型钙离子电池
2018-04-25 11:50
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
专题
相关新闻
-
韩国研发单原子铂催化剂 可让燃料电池在700摄氏度高温下工作
2020-11-06 09:48 -
研究团队探讨固态电池工作极限 以提升电动汽车续驶里程
2020-11-03 09:03 -
-60℃充电!高性能低温锂金属电池
2020-09-21 11:59 -
美国研发可在零下10摄氏度工作的锂金属电池
2020-08-25 17:33 -
斯坦福研发阻燃固态电池:着火后依然正常供电
2020-03-15 15:22 -
青岛能源所揭示出下一代锂金属电极的工作机制
2019-12-18 10:48 -
科学家提出新型预锂化策略用于提升锂离子电池在宽工作温区下的性能
2019-10-21 21:33 -
研究人员研发新型电解质 扩大锂离子电池的工作温度范围
2019-07-11 10:29
本月热点
-
2020年锂电池行业研究报告
2021-05-11 11:24 -
突发|深圳一锂电企业停止经营、解散员工!
2021-05-11 10:02 -
4月我国动力电池装车量同比上升134.0%
2021-05-13 08:26 -
如何看待Pack内铁锂和三元混用
2021-06-01 09:25 -
可充电中性锌空气电池:进展,挑战和未来
2021-05-19 10:59 -
揭开赣锋锂业的家底
2021-06-03 09:46 -
“电池荒”来袭,生产纯电动汽车的车企要被卡脖子了?
2021-06-01 21:22 -
关于征集《锂离子电池用连续式真空干燥系统技术规范》等两项行业标准的函)征求意见程序
2021-05-31 22:53
 企业微信号
企业微信号 微信公众号
微信公众号









